Questions UE1 2021-2022
Citation de admin le 16 mars 2021, 9h36Hello !
C'est ici que vous pouvez poser toutes vos questions en UE1
Rappel : avant de poser une question, vérifiez bien que celle-ci n'ai pas déjà été posée via la barre de recherche(c'est super rapide, procédez par mots-clés !)
Bon courage à toutes et tous !
Hello ! ![]()
C'est ici que vous pouvez poser toutes vos questions en UE1
Rappel : avant de poser une question, vérifiez bien que celle-ci n'ai pas déjà été posée via la barre de recherche  (c'est super rapide, procédez par mots-clés !)
(c'est super rapide, procédez par mots-clés !)
Bon courage à toutes et tous !
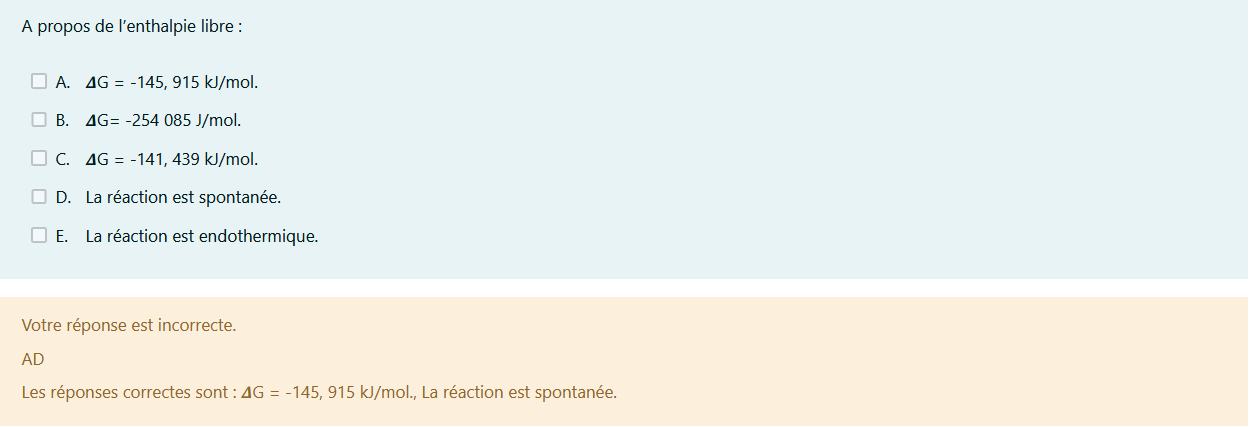
Citation de Remsito le 13 octobre 2021, 14h53Salut, je n'ai pas compris comment calculer l'enthalpie libre, il y a eu une question à propos de cela dans un tutorat mais la réponse n'a pas été justifié. La formule dans mon cours est enthalpie libre = enthalpie - T*entropie mais je ne vois pas comment m'en servir. En espérant que vous pourrez m'aider, merci.
Je vous met aussi l'énoncé qui correspondait ( on trouve 𝜟ST2= -145 J/K/mol. si cela est utile pour l'enthalpie libre)
Salut, je n'ai pas compris comment calculer l'enthalpie libre, il y a eu une question à propos de cela dans un tutorat mais la réponse n'a pas été justifié. La formule dans mon cours est enthalpie libre = enthalpie - T*entropie mais je ne vois pas comment m'en servir. En espérant que vous pourrez m'aider, merci.
Je vous met aussi l'énoncé qui correspondait ( on trouve 𝜟ST2= -145 J/K/mol. si cela est utile pour l'enthalpie libre)

Citation de 110gr le 13 octobre 2021, 20h49Citation de Remsito le 13 octobre 2021, 14h53Salut, je n'ai pas compris comment calculer l'enthalpie libre, il y a eu une question à propos de cela dans un tutorat mais la réponse n'a pas été justifié. La formule dans mon cours est enthalpie libre = enthalpie - T*entropie mais je ne vois pas comment m'en servir. En espérant que vous pourrez m'aider, merci.
Je vous met aussi l'énoncé qui correspondait ( on trouve 𝜟ST2= -145 J/K/mol. si cela est utile pour l'enthalpie libre)
Salut !
Je te remet ici l'intégralité de la correction (à laquelle tu as accès sur le drive du tutorat, je te remet le lien ici : https://drive.google.com/drive/folders/178vGu-3aiwEZwL8tV5Rw9EvcDpWSzxZl?usp=sharing)
Pour trouver 𝜟H, il faut multiplier les 𝜟H de chacun des réactifs et produits par son coefficient stoechiométrique (signés ! : Moins si c'est un réactif et plus si c'est un produit).
J'espère que cette correction va t'éclairer, sinon n'hésite pas à nous rappeler à l'aide 😉
Bonne soirée,
110gr
Citation de Remsito le 13 octobre 2021, 14h53Salut, je n'ai pas compris comment calculer l'enthalpie libre, il y a eu une question à propos de cela dans un tutorat mais la réponse n'a pas été justifié. La formule dans mon cours est enthalpie libre = enthalpie - T*entropie mais je ne vois pas comment m'en servir. En espérant que vous pourrez m'aider, merci.
Je vous met aussi l'énoncé qui correspondait ( on trouve 𝜟ST2= -145 J/K/mol. si cela est utile pour l'enthalpie libre)
Salut !
Je te remet ici l'intégralité de la correction (à laquelle tu as accès sur le drive du tutorat, je te remet le lien ici : https://drive.google.com/drive/folders/178vGu-3aiwEZwL8tV5Rw9EvcDpWSzxZl?usp=sharing)
Pour trouver 𝜟H, il faut multiplier les 𝜟H de chacun des réactifs et produits par son coefficient stoechiométrique (signés ! : Moins si c'est un réactif et plus si c'est un produit).
J'espère que cette correction va t'éclairer, sinon n'hésite pas à nous rappeler à l'aide 😉
Bonne soirée,
110gr
Fichiers téléversés :- Vous devez vous connecter pour avoir accès aux fichiers mis en ligne (uploadés).
